2025年5月,高章华团队在期刊《Organic Letters》(中科院1区,IF=5.0)发表题为“2‐Pyridone-Enhanced Mn-Catalysis for the Synthesis of ortho-Deuterated Aromatic Nitriles”的研究性论文。
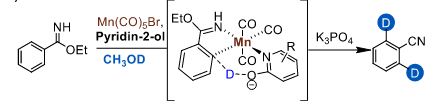
团队提出了一种以Mn(CO)5Br为催化剂,CH3OD为氘源合成邻位氘代芳腈的方法,其中芳基亚胺酸酯的结构用于与氰基的相互转化。该方法具有广泛的底物范围和优异的官能团耐受性,允许各种复杂分子的后期修饰,具有良好的产率和氘代掺入。机理研究表明,2-吡啶酮对该化学的成功至关重要,可作为增强氢同位素交换速率的内源性碱。
研究从优化苯乙酮亚氨酸酯的氘代开始,在20 mol% Mn(CO)5Br催化剂存在下,以20 mol%的5-甲基-2羟基吡啶、2当量的NaOPiv和氘源CH3OD,100℃反应2 h,以90%的收率得到氘代亚氨酸酯,氘代度为1.7 DMS。在已优化的条件下,进行了底物拓展。苯环上的多种常见官能团,包括烷基(甲基、异丙基、叔丁基和三氟甲基)、甲氧基、苯基、卤素(F、Cl、Br)、羟基、硝基、乙烯基、甲磺酰基等,都被发现能够以较好的收率和氘代合成所需的氘代芳腈。腈基邻位或对位不同取代基的电子性质不影响产率或氘代,但苯环上的大位阻基团对HIE反应影响显著。此外,其他带有萘基和杂环基团的亚胺酸酯也可用于该反应,以高产率提供氘代腈和氘代物。为了进一步评价该反应的实用性,对部分药物进行了邻位导向的HIE,并成功对吡仑帕奈、来曲唑前药和西酞普兰等生物活性分子的后期氘代。除邻位氘代外,药物的其他活性中心,包括杂芳环和苄位C-H键也有一定程度的氘代。为了说明当前方案的合成实用性,团队探索了氘代芳腈的进一步衍生化。在不影响氘代的情况下,以优异的收率得到了邻氘代苯乙酮、4-甲基苯甲酰胺、4-甲基苄胺和4-甲基苯甲酸。
高章华教授团队发展了一种新型的锰吡啶酮催化的各种芳基亚胺酸酯的氘代反应,以CH3OD为氘源合成邻位氘代芳基腈。值得注意的是,2-吡啶酮在该反应的成功中起着至关重要的作用,作为CMD碱促进氢同位素交换。此外,多种芳基腈可以被氘标记,显示出广泛的官能团耐受性和生物活性分子的兼容性。鉴于腈基在药物化合物和有机合成中的广泛存在,这种HIE反应在氘代药物发现中显示出更广阔的应用前景。